热力学第一定律与能量守恒
物质和运动守恒的概念,虽然早在18世纪中叶就已由俄国科学家罗蒙诺索夫提出来了,但是关于热是运动的一种形式、热相机械运动是可以相互转换的概念直到一百多年以后才被物理学家们认识相接受.在此以前,“热素说”还占着统治地位.这种学说认为热是一种待殊的、没有质量的流质,称为“热素”.物体的冷热取决于其中含“热家”的多少.“热素”会从较热的物体流到较冷的物体中去.自然界中存在的热京既不能创造,也不能消灭,即“热素”守恒.。热家说”把热看成是一种物质,否认它是物质运动的一种形式,否认热和物质的其他运动形式之间可以相互转换.虽然运用“热素说”也可以解释不少热现象,但是在蒸汽机发明以后,“热素说”并不能解释热相机械运动之间的关系,它巳成了科学发展的障碍.
最初用实验来驳斥“热素说”的是伦福镕(Coum Rumford,1753一1814)和戴维(HumphryDa”y,1778—1829).伦福镕发现在钻炮筒时,炮筒和铁屑的温度升高,产生大量的热,只要不断地钻,热量就不断产生,因而他断言:“热可由运动产生,它绝不是一种物质.”但是,“热素学”的维护者们提出种种不能成立的说法,企图把伦福德的发现纳入“热素学”的轨道,死守他们的信条.1799年,戴维在伦福镕的启示下,进行了一个很有说服力的实验:他用两块冰在空中摩擦,并巳使周围的温度低于冰块的温度,最后冰块化成了水.裁维的实验证明,由冰变水所需要的热量不可能是由外面进入的“热素”,因为周围的温度更低,也不可能是由于比热变化而放出的“热素”,因为水的比热要比冰高.这个实验雄辩地证明了
“热京说”的错误,可惜的是,伦福德和戴继都没有找到热量和功的
数量关免
N42年,德国医生迈耶(J.R.M,y6r,1614一1878)发表了—‘篇论文,提出能量守恒的理论,认为热是能的一种形式,可与机械能相互转换,并从空气的定压比热和定容比热之差算出了热功当量.因为这不是直接的实验数据,他的理论还没有被当时的物理学界承认.热力学第一定律的最后奠定要归功于英国物理学家焦耳(J.P.JoMLe,1818一l 889),他前后共用了二十多年时间,通过各种不同的方法测定热功当量,得到了一致的结果.到l 850年,他的实验结果已使科学界公认了能量守恒定律的正确性.
热力学第一定律就是能量守恒定律,它有很多表达方式,
例如:
热是能的一种、机械能变热能或热能变机械能的时候,它们的比值是一定的.
热可以变为功,功也可以变为热,一定量的热消失时,必产生一定量的功;消耗了一定量的功时,必出现与之对应的一定量的热.
当—个体系的状态经过一个循环的变化后,对这个体系所加入的热量的代数相等于体系向外作功的代数和,它的数学表达式为
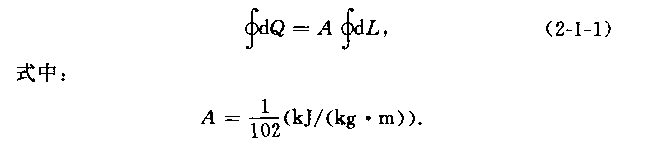
热力学第一定律还有一个简单的表达形式:第一类永动机是
不可能制成的.


